版本:國家藥品監督管理局2002年公佈的第二批化學藥品說明書鍀[99mTc]植酸鹽注射液說明書由國家藥品監督管理局於2002年02月05日藥監注函[2002]58號《關於公佈第二批化學藥品說明書目錄的通知》發佈。國家藥品監督管理局公佈的說明書是規範修訂後的建議參考樣稿,企業如有疑異,可提出修改意見。〔適應症〕應與原批准的內容一致;〔不良反應〕、〔藥物相互作用〕等項內容,企業提供的說明書不能比樣稿所列的少。對於說明書樣稿中的空項或未列全的項目,應要求企業根據實際情況填寫,如商品名、規格等。
鍀[99mTc]植酸鹽注射液說明書
【藥品名稱】
通用名:鍀[99mTc]植酸鹽注射液
曾用名:
商品名:
英文名:Technetium[99mTc] Phytate Injection(99mTc-Phy)
漢語拼音:De[99mTc]zhisuɑnyɑn Zhusheye
結構式:
分子式:
分子量:
【性狀】
本品爲無色澄明液體。
【藥理毒理】
99mTc-植酸鹽在血液中與鈣離子螯合,形成不溶性99mTc-植酸鈣膠體顆粒,直徑20~40nm,由網狀內皮系統從血中清除,90%聚集在肝臟的枯否細胞內,2%~3%進入脾,8%進入骨髓。因此可使肝顯像,而肝內的佔位性、破壞性或缺血性病變,不能濃聚植酸鈣膠體顆粒,故出現放射性減低區或缺損區,病變乃得以顯示。肝功能明顯低下時,脾和骨髓內代償性濃聚增加此,有時甚至肺亦顯影。當脾功能亢進時,也有程度不同的顯影。
LD50爲12mg/kg,約爲成人一次用量(按公斤體重計算)的600倍。
【藥代動力學】
靜脈注射後,與血液中的鈣離子螯合形成99mTc-植酸鈣膠體,正常時約90%被肝臟枯否細胞作爲異物吞噬,其餘部分被脾、淋巴結、骨髓等部位的單核吞噬細胞吞噬。膠體顆粒被吸收後,不從細胞內排出,未與植酸鈉結合的99mTcO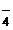 和少量從膠體顆粒落下來的99mTc經尿排出,24小時內約排出11%。
和少量從膠體顆粒落下來的99mTc經尿排出,24小時內約排出11%。
【適應症】
診斷用藥。主要用於肝、脾及骨髓顯像。
【用法用量】
靜脈注射99mTc植酸鹽111~185MBq(3~5mCi)後5~10分鐘即可開始檢查。肝功能差的病人檢查的時間應適當推遲。一般常用前後位、右側位及後前位檢查,必要時可加用斜位及左側位。
【不良反應】
【禁忌】
【注意事項】
99mTc植酸鹽的毒性極低,病人檢查時僅需要數毫克植酸鹽,正常人血清中鈣的含量約爲10mg/100mg,這樣,消耗的鈣是微不足道的。本品如發生變色或沉澱應停止使用。
【孕婦及哺乳期婦女用藥】
孕婦禁用,哺乳期婦女慎用。
【兒童用藥】
慎用。
【老年患者用藥】
【藥物相互作用】
尚不明確。
【藥物過量】
【規格】
【貯藏】
【包裝】
【有效期】
【批准文號】
【生產企業】
企業名稱:
地 址:
郵政編碼:
電話號碼:
傳真號碼:
網 址: